研究内容
プロジェクト3−2(4)
私たちは、肝臓細胞・脂肪細胞・筋肉細胞といったインスリンの標的細胞を用いて、いろいろなホルモン・成長因子・サイトカイン・栄養因子などによるインスリンの細胞内シグナルの抑制機構を解析してきました。この研究の過程で、私たちは、脂肪細胞や筋肉細胞におけるインスリン抵抗性の少なくとも一部は、インスリン細胞内情報伝達経路の種々の段階に障害が生じて、標的にシグナルが伝わらなくなることが原因であることを突き止めました。
例えば、3T3-L1脂肪細胞を用いた解析の結果、アディポサイトカインであるTNFαや遊離脂肪酸による長時間処理は、インスリン依存性IRSのチロシンリン酸化を抑制する、酸化ストレスはインスリン依存性 PI 3-kinaseの活性化を抑制する、成長ホルモン(GH)長時間処理は、糖の取り込みを仲介するグルコース輸送体(GLUT)のうちGLUT4が細胞膜へ移行するのにも関わらず、糖の取り込みが阻害されることなどが明らかとなりました (図)。 このように、インスリン抵抗性発生因子が、それぞれ異なる段階に作用してインスリン抵抗性を発生させることがわかってきましたが、私たちは、これらの作用点の違いが、生体の恒常性維持においてそれぞれの因子により発生するインスリン抵抗性の持つ意義を示しているものと考えています。特に、いろいろな因子によって作用点が異なることは、それぞれの因子の情報をシグナル系の違う段階に入力することにより情報を統合し、インスリン活性のファインチューニングを可能にしていると説明することもできます。このプロジェクトでは、それぞれの因子によるインスリン抵抗性の複雑な発生機序を分子レベルで解明し、インスリン抵抗性を解除する薬剤開発のための分子的基礎を確立するのが、私たちの研究の目標です。
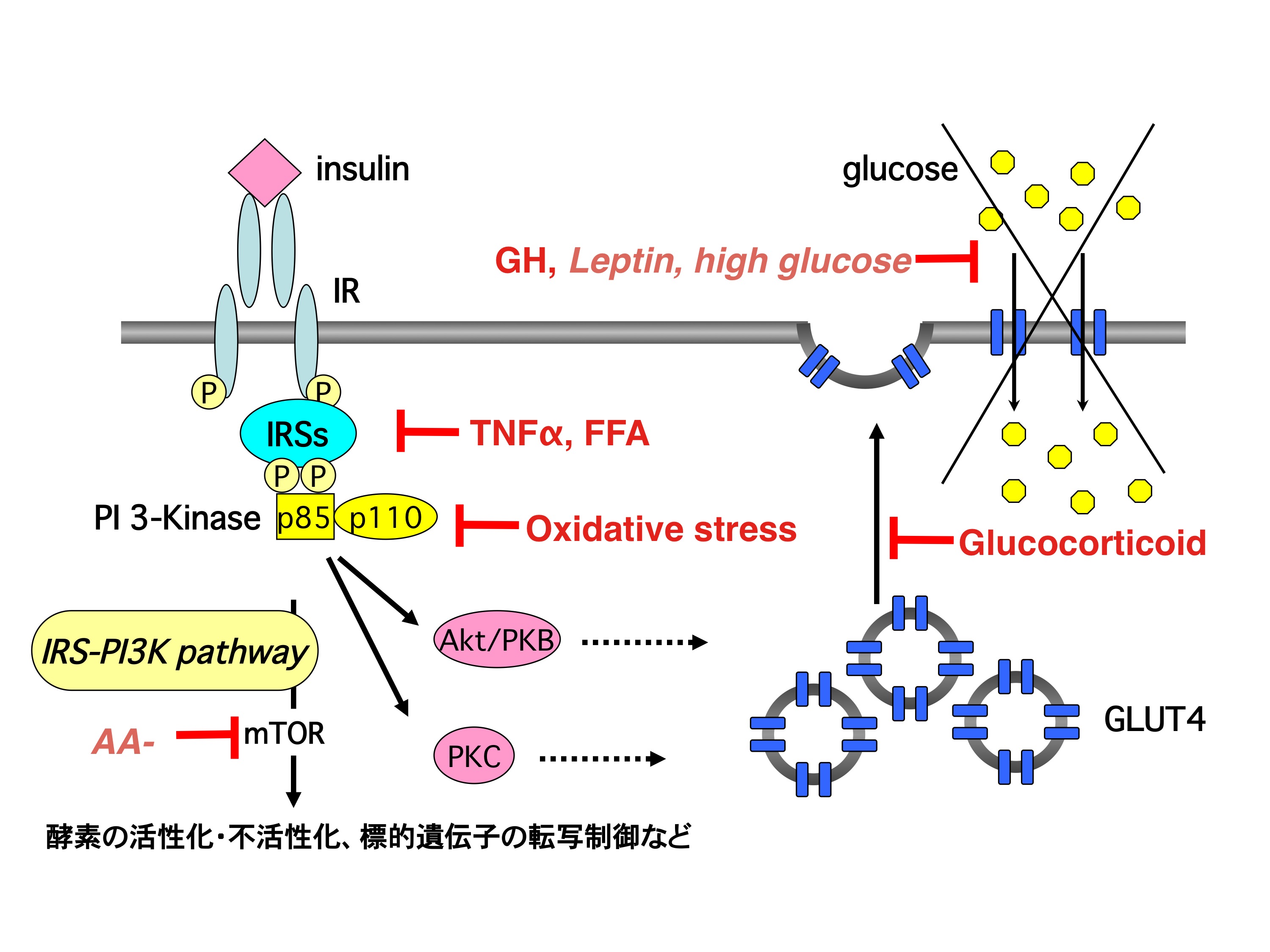
インスリンシグナルを抑制するステップ
インスリン抵抗性を発生させると考えられる分子は多数あることは先に述べたが、インスリンシグナル伝達の異なる段階に影響することが明らかになりつつある。例えば、TNFαや遊離脂肪酸はIRSのチロシンリン酸化を抑制、酸化ストレスはPI 3kinaseの活性化を抑制、glucocorticoidはGLUT4が含まれているvesicleが細胞膜へ移動する段階を阻害する。更に、成長ホルモンは、GLUT4は細胞膜存在するにもかかわらず、糖の取り込みを阻害する。このようにインスリン様シグナル伝達の異なる段階で他の因子とのクロストークが起こる結果、インスリン抵抗性、あるいはIGF抵抗性が起こると考えられる。
| 研究内容:目次 | プロジェクト3−2(3) 戻る 次へ プロジェクト3−2(5) |