研究内容
プロジェクト1(3)
一方、同じ細胞系において、IGFは、細胞増殖と細胞分化を誘導することが報告されていますが、どのような因子のどのようなシグナルクロストークを介して、細胞増殖や細胞分化、それぞれを誘導するのかについては、ほとんど明らかにされていません。そこで、私たちは、3T3-L1脂肪前駆細胞の増殖、分化過程におけるIGFシグナルの変動について解析を進めました。その結果、増殖期には、IGF-Iレセプター量が多く、ShcとIRS-2がIGFシグナル伝達に重要な役割を果たしているのに対して、グルココルチコイドやエピネフリンにより分化進行が決定される初期には、Shcが徐々に減少、更に一時的にIRS-1が著減しIGFシグナルが減弱することが分化誘導に必須であることが明らかになってきました。この際、IRS-2のチロシンリン酸化は逆に増加し、この生理的意義にも興味が持たれるところです。その後、IGF-Iレセプターが減少し、代わりにインスリンレセプター、IRS-1が増加、インスリン依存性活性が発現できるように成熟が進み、脂肪蓄積が起こる、すなわち脂肪細胞として機能ができるようになります。このように、増殖と分化において異なるシグナル系が異なる様式でIGF/インスリンの情報を細胞に伝えていることがわかってきました (図9)。
一方、間葉系の幹細胞から、脂肪細胞と筋肉細胞は分化することは広く知られていますが、筋芽細胞の分化にもIGFは必須であることが知られています。筋芽細胞の分化過程においては、脂肪細胞に観察されたようなIRS-1の著減は観察されていませんが、IRS-1を過剰発現すると細胞分化が誘導されなくなり、分化誘導にはやはりIRSを介したIGFシグナルの減弱が必要と考えられました (図9)。 これらの結果をふまえ、現在、成人の幹細胞と考えられている筋衛星細胞を用いて、IGFによる脂肪細胞、筋肉細胞への選択的な分化制御の試みを進めています。最近になり、インスリンのシグナルに 応答して細胞質と核の間を移動することが知られているFoxO1という転写因子が、核内にあると筋管細胞に、核外にあると脂肪細胞に分化することが明らかとなっています。
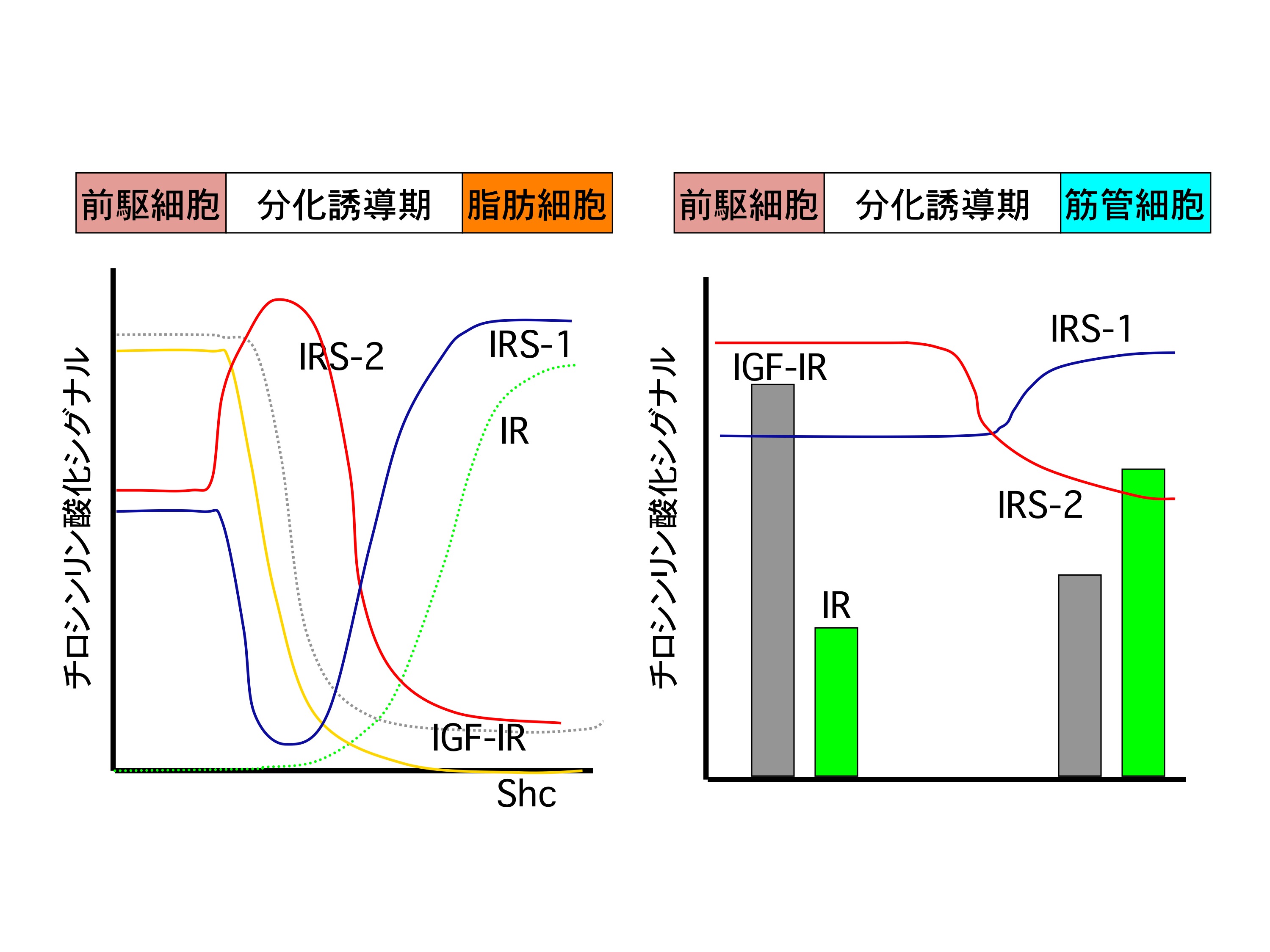
マウス3T3-L1脂肪前駆細胞を、glucocorticoid、cAMP存在下で、IGFで処理すると、脂肪細胞への分化が誘導される。分化誘導の過程で、IRS-1のチロシンリン酸化が激減し、代わりにIRS-2のチロシンリン酸化が増加する。分化誘導の進行に伴い、IRS-1のチロシン化が回復し、IRS-2のチロシンリン酸化が抑制すると同時に、IGF-Iレセプターがダウンレギュレーション、逆にインスリンレセプターがアップレギュレーションする。これら一連のインスリン様シグナルの変化が、脂肪細胞への分化に必須と考えられている(左図)。一方、ラットL6筋芽細胞、マウスC2C12細胞を、IGFで処理すると、やはり筋管細胞への分化が誘導される。この際には、IRS-1のチロシンリン酸化には脂肪細胞の分化過程のような変化が観察されない(右図)。このように、間葉系幹細胞から脂肪細胞・筋管細胞への分化には、細胞が置かれている状況によってインスリン様シグナルが異なる様式で調節され、その運命が決定される可能性が考えられる。
| 研究内容:目次 | プロジェクト1(2) 戻る 次へ プロジェクト1(4) |